Węglowodory nienasycone
Węglowodory nienasycone - mają w cząsteczce wiązania podwójne C=C lub potrójne C≡C.
Alkeny
Alkeny to organiczne związki chemiczne, które należą do grupy węglowodorów. To oznacza, że są zbudowane tylko z dwóch pierwiastków: węgla (C) i wodoru (H).
Cechą, która wyróżnia alkeny spośród innych węglowodorów, jest obecność podwójnego wiązania między dwoma atomami węgla C=C. Takie wiązanie sprawia, że alkeny mają inne właściwości niż na przykład alkany (czyli węglowodory, które mają tylko pojedyncze wiązania między atomami węgla C−C).
Alkeny to węglowodory zawierające podwójne wiązanie między dwoma atomami węgla. Są zbudowane z atomów węgla (C) i wodoru (H).
Alkeny mają podwójne wiązanie między atomami węgla C=C, podczas gdy alkany mają tylko pojedyncze wiązania C−C.
Nazwę alkenu rozpoznaje się po końcówce −en.
Wzór ogólny szeregu homologicznego alkenów CnH2n
| nazwa | wzór sumaryczny | wzór półstrukturalny | wzór strukturalny |
| eten (etylen) | C2H4 | CH2=CH2 | 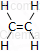 |
| propen | C3H6 | CH2=CH−CH3 | 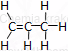 |
| buten | C4H8 | CH2=CH−CH2−CH3 | 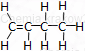 |
Właściwości fizyczne etenu (C₂H₄):
- Stan skupienia: Gaz w warunkach normalnych (temperatura pokojowa i ciśnienie atmosferyczne).
- Kolor i zapach: Bezbarwny, o słodkawym zapachu.
- Rozpuszczalność: Słabo rozpuszczalny w wodzie, dobrze rozpuszcza się w rozpuszczalnikach organicznych, takich jak benzen czy eter.
- Temperatura topnienia: -169,4°C.
- Temperatura wrzenia: -103,7°C.
- Gęstość: Mniejsza od gęstości powietrza (ok. 1,26 g/L przy 0°C i 1 atm).
Reakcje spalania etenu
| C2H4 + 3O2 → 2CO2 + 2H2O | spalanie całkowite |
| C2H4 + 2O2 → 2CO + 2H2O | spalanie niecałkowite (półspalanie) |
| C2H4 + O2 → 2C + 2H2O | spalanie niecałkowite |
Reakcje przyłączania (addycji)
Przyłączenie (addycja), to proces chemiczny, w którym dwa reagenty łączą się, tworząc jeden nowy produkt. Jest charakterystyczne dla związków nienasyconych, takich jak alkeny (z podwójnym wiązaniem) czy alkiny (z potrójnym wiązaniem). W reakcji addycji cząsteczki reagenta „przyłączają się” do cząsteczki związków nienasyconych, otwierając jej wiązania podwójne lub potrójne.
Przyłączenie wodoru (addycja wodoru)
Reakcja addycji między etenem (C₂H₄) a wodorem (H₂) to reakcja, w której podwójne wiązanie w etenie zostaje zerwane, a atomy wodoru przyłączają się do węgla, tworząc etan (C₂H₆). W wyniku tego procesu związek nienasycony staje się nasycony.
C2H4 + H2 → C2H6
CH2=CH2 + H2 → CH3−CH3
eten etan

Przyłączanie bromu (addycja bromu)
C2H4 + Br2 → C2H4Br2
CH2=CH2 + Br2 → CH2Br−CH2Br
eten + brom → 1,2-dibromoetan
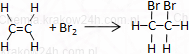
Polimeryzacja etenu
Polimeryzacja - reakcja łączenia dużej ilości cząsteczek związków nienasyconych (merów) i tworzenie związku wielkocząsteczkowego (polimeru)
n CH2=CH2 → -[−CH2−CH2−]−n
eten polieten (polietylen)

Alkiny
Alkiny to kolejna grupa węglowodorów, która różni się od alkenów i alkanów. Zawierają one potrójne wiązanie między dwoma atomami węgla C≡C, co sprawia, że są jeszcze bardziej reaktywne.
Wzór ogólny CnH2n-2, W nazwie posiadają końcówkę -yn.
| nazwa | wzór sumaryczny | wzór półstrukturalny | wzór strukturalny |
| etyn (acetylen) | C2H2 | HC≡CH | H−C≡C−H |
| propyn | C3H4 | HC≡C−CH3 | 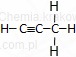 |
| butyn | C4H6 | HC≡C−CH2−CH3 | 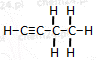 |
Właściwości fizyczne etynu (C₂H₂):
- Stan skupienia: Gaz w warunkach normalnych.
- Kolor i zapach: Bezbarwny; czysty etyn jest bezwonny, ale techniczny może mieć nieprzyjemny zapach z powodu zanieczyszczeń (np. siarkowodorem).
- Rozpuszczalność: Słabo rozpuszczalny w wodzie, dobrze rozpuszcza się w rozpuszczalnikach organicznych, takich jak aceton czy etanol.
- Temperatura topnienia: -80,8°C.
- Temperatura wrzenia: -84°C.
- Gęstość: Mniejsza od gęstości powietrza (ok. 1,17 g/L przy 0°C i 1 atm).
Reakcje spalania etynu
2C2H2 + 5O2 → 4CO2 + 2H2O
2C2H2 + 3O2 → 4CO + 2H2O
2C2H2 + O2 → 4C + 2H2O
Reakcje przyłączania (addycji)
Reakcja etynu z wodorem
HC≡CH + H2 → CH2=CH2 (eten)
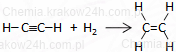
HC≡CH + 2H2 → CH3−CH3 (etan)
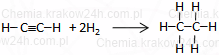
Reakcja etynu z bromem
HC≡CH + Br2 → CHBr=CHBr
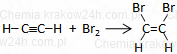
HC≡CH + 2Br2 → CHBr2−CHBr2

Metoda odróżniania węglowodorów nasyconych i nienasyconych
Węglowodory nasycone i nienasycone różnią się między sobą obecnością wiązań podwójnych lub potrójnych. Węglowodory nasycone (alkany) mają tylko pojedyncze wiązania między atomami węgla, natomiast węglowodory nienasycone (alkeny, alkiny) zawierają co najmniej jedno wiązanie podwójne (w alkenach) lub potrójne (w alkinach).
Jedną z metod odróżniania węglowodorów nasyconych od nienasyconych jest reakcja z wodą bromową (Br₂). Brom reaguje z wiązaniem podwójnym lub potrójnym w cząsteczkach węglowodorów nienasyconych, powodując odbarwienie roztworu.
-
Węglowodory nasycone (alkany):
Alkany nie reagują z wodą bromową i nie zachodzi odbarwienie roztworu. Woda bromowa zachowa swoją barwę pomarańczową lub czerwoną. -
Węglowodory nienasycone (alkeny i alkiny):
Alkeny i alkiny reagują z wodą bromową, powodując odbarwienie roztworu bromu (brom przestaje być widoczny). Reakcja ta odbywa się przez dodanie bromu do wiązania wielokrotnego.
Zastosowania etenu (C₂H₄):
Eten i dojrzewanie owoców:
- Kiedy w sklepach sprzedawane są banany, które jeszcze nie są do końca dojrzałe, często są one przechowywane w specjalnych pomieszczeniach z etenem. Ten gaz pomaga przyspieszyć dojrzewanie owoców, dzięki czemu stają się one bardziej słodkie i miękkie w krótszym czasie.
- Kiedy banan, który w naszym domu leży obok jabłka, zaczyna szybciej dojrzewać, bo jabłko naturalnie emituje eten.
Produkcja tworzyw sztucznych:
- Eten jest używany do produkcji polietylenu, który jest tworzywem sztucznym wykorzystywanym do produkcji wielu przedmiotów, które mamy w domu – od plastikowych butelek po torby na zakupy.
- Większość plastikowych butelek, które widzimy w sklepach, a także opakowania na żywność, wykonane są właśnie z tego materiału, który powstaje z etenu.
- Eten jest kluczowym surowcem do wytwarzania polietylenu (PE), który znajduje zastosowanie w produkcji opakowań, worków foliowych, rur, czy zabawek.
Zastosowania etynu (C₂H₂):
Etyn i spawanie metali
- Etyn, czyli acetylen, jest gazem wykorzystywanym w palnikach, które są używane do spawania metali. Dzięki bardzo wysokiej temperaturze spalania etyn jest nieocenionym surowcem w przemyśle budowlanym i motoryzacyjnym, zwłaszcza przy naprawach starych samochodów.
- Gdy naprawiamy coś w domu – na przykład łączymy metalowe elementy. Choć nie używamy etynu, to w przemyśle technicznym takie spawanie jest powszechnie stosowane i umożliwia naprawę uszkodzonych przedmiotów.
Etyn i przemysł chemiczny:
- Etyn wykorzystywany jest także do produkcji takich rzeczy jak kleje, farby i tworzywa sztuczne, które spotykamy na co dzień – w naszych domach, szkołach, czy biurach.
- Warto dodać, że gdy używamy kleju do naprawy butów czy tapet, nie zdajemy sobie sprawy, że składniki tych produktów mogą pochodzić właśnie z etynu.
Oba węglowodory, eten i etyn, mają ogromne znaczenie w przemyśle chemicznym, choć ich zastosowania różnią się ze względu na odmienną budowę chemiczną i właściwości fizyczne.
Zastosowania polietylenu (PE):
Polietylen to jedno z najpowszechniej używanych tworzyw sztucznych, cenione za swoją wszechstronność, lekkość i odporność chemiczną. W zależności od gęstości i struktury molekularnej wyróżnia się kilka rodzajów polietylenu, takich jak polietylen wysokiej gęstości (HDPE), niskiej gęstości (LDPE), liniowy niskiej gęstości (LLDPE) i inne. Oto jego główne zastosowania:
1. Opakowania:
- Folie i worki plastikowe: używane w sklepach spożywczych, jako opakowania na produkty, torebki na zakupy.
- Butelki i pojemniki: szczególnie z HDPE, stosowane na mleko, detergenty, kosmetyki i inne płyny.
- Opakowania ochronne: w przemyśle spożywczym i farmaceutycznym do zabezpieczenia produktów.
2. Budownictwo:
- Rury: HDPE jest wykorzystywany do produkcji rur kanalizacyjnych, wodociągowych oraz gazowych dzięki odporności na korozję i wytrzymałości mechanicznej.
- Izolacje kabli i przewodów: dzięki dobrej izolacji elektrycznej i odporności na wilgoć.
- Folie ochronne i membrany: stosowane w hydroizolacjach dachów, fundamentów i tarasów.
3. Przemysł motoryzacyjny:
- Zbiorniki na paliwo: lekkie, wytrzymałe zbiorniki wykonane z HDPE.
- Osłony i elementy karoserii: używane w samochodach i innych pojazdach.
4. Rolnictwo i ogrodnictwo:
- Folie do upraw: chroniące przed chwastami, promieniowaniem UV i utratą wilgoci.
- Rury nawadniające: odporne na działanie wody i czynników chemicznych.
- Sznurki i siatki rolnicze: stosowane do pakowania lub ochrony roślin.
5. Sprzęt gospodarstwa domowego:
- Pojemniki do przechowywania żywności: odporne na działanie temperatury i chemikaliów.
- Akcesoria kuchenne: miski, deski do krojenia, osłonki ochronne.
6. Zastosowania medyczne i farmaceutyczne:
- Strzykawki jednorazowe: produkowane z materiałów zgodnych z wymaganiami medycznymi.
- Opakowania leków: bezpieczne i trwałe.
- Worki do przechowywania krwi i innych płynów biologicznych.
7. Przemysł sportowy i rekreacyjny:
- Deski surfingowe i kajaki: wykonane z wytrzymałego i odpornego na uderzenia HDPE.
- Meble ogrodowe: lekkie, trwałe i odporne na czynniki atmosferyczne.
8. Recykling i inne zastosowania ekologiczne:
- Worki na śmieci: z LDPE i LLDPE, często pochodzące z recyklingu.
- Elementy infrastruktury recyklingowej: takie jak pojemniki na odpady czy kosze na śmieci.
Polietylen znajduje zastosowanie w niemal każdej dziedzinie życia dzięki swojej wszechstronności, dostępności i szerokim możliwościom przetwórstwa. Jego wadą jest trudna degradacja, dlatego coraz częściej promowane są jego recykling i rozwój biodegradowalnych alternatyw.
Izomeria i izomery
Izomeria to zjawisko polegające na tym, że istnieje więcej niż jedna cząsteczka o tym samym wzorze sumarycznym, ale różniąca się strukturą chemiczną lub sposobem rozmieszczenia atomów w cząsteczce. Izomery to związki chemiczne, które mają ten sam wzór sumaryczny, ale różnią się między sobą właściwościami chemicznymi i fizycznymi.
Izomer to jedna z różnych form tego samego związku chemicznego, które mają ten sam wzór sumaryczny, ale różnią się układem atomów w cząsteczce.
Izomeria położenia wiązania wielokrotnego
Izomeria położenia wiązania wielokrotnego dotyczy związków, które mają identyczny wzór sumaryczny, ale różne położenie podwójnego lub potrójnego wiązania w łańcuchu węglowym. Jest to rodzaj izomerii strukturalnej, w której różnice polegają na tym, że wiązanie wielokrotne znajduje się w innym miejscu w cząsteczce.
Przykład:
Rozważmy dwa izomery etenu, który ma wzór sumaryczny C₄H₆:
-
But-1-en (C₄H₆):
CH2=CH−CH2−CH3
Wiązanie podwójne znajduje się między pierwszym a drugim atomem węgla: -
But-2-en (C₄H₆):
CH3−CH=CH−CH3
Wiązanie podwójne znajduje się między drugim a trzecim atomem węgla:
Mimo że oba izomery mają ten sam wzór sumaryczny (C₄H₆), różnią się miejscem, w którym występuje podwójne wiązanie (1-węgiel vs 2-węgiel). To jest właśnie przykład izomerii położenia wiązania wielokrotnego.
Podsumowanie:
Izomeria położenia wiązania wielokrotnego to rodzaj izomerii, w której różne związki mają ten sam wzór sumaryczny, ale różnią się lokalizacją wiązania wielokrotnego (np. podwójnego) w łańcuchu węglowym. Izomery takie mają różne właściwości chemiczne i fizyczne.
